蛋白质是由称为氨基酸的较小成分组成的长聚合物,在人体功能中起着至关重要的作用。在人类的一生中,这些蛋白质“串”折叠成独特的3D结构或构象,这种折叠过程会影响大脑中不同通道和受体与其他蛋白质的相互作用。
随着人类年龄的增长,基因突变和环境因素会导致蛋白质的错误折叠。神经退行性疾病,如阿尔茨海默病和帕金森病,现在已知是由蛋白质不正确的“折叠”引起的。
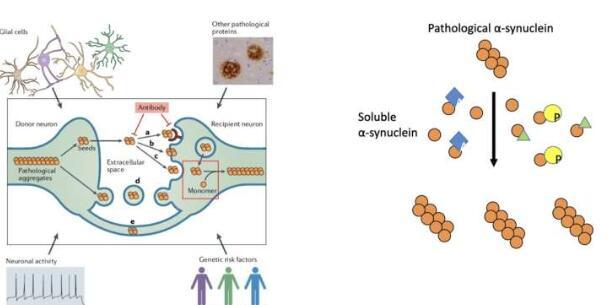
加州大学洛杉矶分校(UCLA)、宾夕法尼亚大学以及美国和中国其他研究所的一组研究人员最近发现了一种调节病理蛋白(错误折叠α-突触核蛋白)传播的机制,该蛋白被发现与帕金森病的进展有关。这种机制在发表在《自然神经科学》上的一篇论文中概述,包括细胞对这些蛋白质的一系列改变,这会影响它们在大脑中扩散的能力。
“当我为该领域撰写评论时,这篇论文的整个想法就发展起来了,我总结了病理蛋白传播的所有已知机制,”进行这项研究的研究人员之一Chao Peng告诉Medical Xpress。
“在我写这篇文章的时候,我注意到目前对病理蛋白传递的研究主要集中在病理蛋白或'种子'上。然而,病理蛋白的成功传播不仅需要病理蛋白(种子),还需要相应的正常可溶性蛋白(底物)。
过去大多数专注于蛋白质和神经退行性疾病的神经科学研究都没有探索可溶性蛋白质调节病理蛋白扩增的机制。Peng和他的同事最近工作的主要目标是研究这些影响,特别是关注蛋白质α-突触核蛋白(a-syn),当错误折叠时,它与帕金森病的进展有关。
“在a-syn上发现了许多翻译后修饰(PTM),其中许多也在可溶性a-syn上被发现,”彭说。“因此,我们决定测试可溶性a-syn PTM是否会调节病理性a-syn的扩增。因此,我们开发了一种基于细胞的测定方法,可以用来模拟细胞中的这种扩增过程。
在他们的实验中,研究人员使用了蛋白质a-syn的病理版本,该蛋白质与在不同神经退行性疾病患者中观察到的蛋白质相匹配。然后,他们分析了这些病理性a-syn蛋白在不同疾病中的扩增。
总体而言,Peng及其同事收集的研究结果确定了一种新的机制,通过该机制,可溶的,改变的a-syn蛋白影响病理性a-syn的扩增,这种蛋白质与帕金森氏症和其他神经退行性疾病的进展有关。因此,在未来,它们可以激发探索这种新发现机制的其他研究,同时也有可能为新的靶向治疗干预措施的开发提供信息。
“我们的研究是第一个分析可溶性蛋白质如何调节病理蛋白扩增的研究,这代表了调节病理蛋白在患病大脑中扩散的全新机制,”彭补充说。“尽管这项研究的重点是a-syn,但我们相信同样的机制也适用于其他与神经退行性疾病相关的病理蛋白。我们现在计划研究可溶性蛋白质如何调节其他神经退行性疾病相关病理蛋白的病理蛋白扩增。
